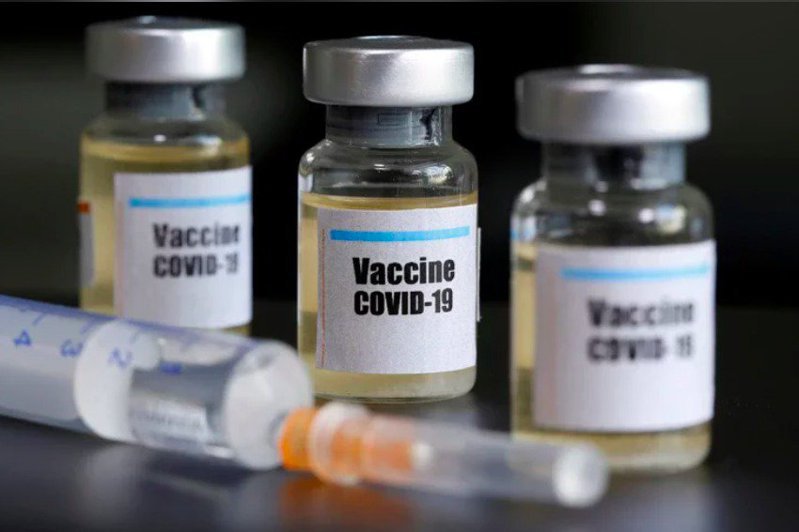
新冠疫苗要做一期、二期、三期和四期临床试验
新冠疫苗在上市之前必须完成以人为对象的三期临床试验。
一期临床:对象有几十人,主要观察安全性的指标,包括急性毒性和慢性毒性指标。
二期临床:涉及几百人,观察免疫原性和安全性指标,研究和评估不同剂量、针次、间隔时间的疗效差异。
三期临床:有成千上万人参与,观察大样本情况下疫苗的有效性和安全性,在流行的人群中,流行的区域中,完成一个流行周期,观察疫苗是否能够防止人感染。
四期临床:上市后并不意味着疫苗万无一失,在实际应用中还要对上市疫苗继续进行临床观察和监控,必要时予以修正。
新冠疫苗三期临床试验的医学原理
完成三期临床是疫苗最终研发成功和被准上市的最为关键的要素。三期临床试验必须按照医学科学的原理和政府监管机构的规定严格地进行,其数据结果和分析论证必须公布,而接受全行业、全社会的学术讨论和伦理评估。
大样本随机双盲对照试验是医学科学试验的基石。新冠疫苗三期临床试验全过程都在该医学原理的指导下严格进行,简述如下。
1)对照:设定一个试验组(使用疫苗),一个对照组(不使用疫苗),最后的有效性来自二组结果的有统计学意义的差异。
2)双盲:试验者(医生)与受试者(试验志愿者)双方都不知道使用的是疫苗还是对照安慰剂。从而排除试验者与受试者主观偏见,最终对试验结果的判断更具客观性。一般临床试验采用双盲法。在实行双盲法有困难时才采用单盲法,即试验者知道分组状况,但受试者不知道。
3)随机:病人分组是随机的,国家、种族、病情、年龄、性别相妨的病人各组平均分配。从而可以有效避免病人由于个体差异、病情轻重等其他因素导致的效果差异。
4)大样本:样本(受试者的数量)足够大,统计结果才能稀释掉那些特殊状况的受试者,也更能逼近真实情况。
新冠疫苗三期临床试验的实际做法
关于疫苗的有效性,在临床前的试验中,通过动物试验已经证明疫苗可能的保护力。又在二期临床试验中,通过检测中和抗体的浓度来间接证明有效性。
三期临床是让新冠疫苗在流行区域完成一个流行周期的有效性测试。通过比较疫苗接种人群和未接种人群出现新冠肺炎病例的情况,才能评价出新冠疫苗的保护效力,即疫苗保护率(Vaccine of protection)。
根据疫苗研发的常规和WHO的要求,新冠疫苗三期临床有下列要求:
1)选择条件:在疫区,至少一个流行季、
2)选择受试者:各人种、各年龄和性别;
3)受试者人数:至少3万人;
4)对照组的发病人数:至少150人;
5)达到疫苗保护率:至少50%;全程免疫后持续至少两个月;
6)副作用:没有严重不良反应;
新冠疫苗问世倒计时
新冠病毒即使顺利通过三期临床试验,耗时也很长。为了控制疫情全球各国科学家紧锣密鼓地加快研发步伐。既要依据科学方法,又要对人类负责。研制需要时间,并带有很大不确定性。如受试者(志愿者)人数的达到,对照组必须有150人被感染,全程免疫后观察二个月以及毒副反应的出现等。
新冠疫苗的问世正倒计时。有的疫苗已经公布三期临床的中期分析(不是最终分析),估计今年内可以完成。期待更多、更有效、更安全的疫苗在正式完成三期临床试验之后,成为人类抗击新冠病毒的有力武器。
(MX)